
Un recente editoriale del New England Journal of Medicine invita i medici a sorvegliare sui possibili errori cognitivi cui li espone la massiccia esposizione a informazioni in arrivo da fonti di varia affidabilità, come è avvenuto nel caso dell'allarme lanciato a marzo sulla potenziale pericolosità delle terapie antipertensive con ACE inibitori e sartani.
Crediti immagine: Anna Shvets/Pexels. Licenza: Pexels License
Durante la Grande depressione, Franklin D. Roosvelt ammoniva: “Assumi un metodo e perseguilo. Se fallisce, ammettilo con franchezza e provane un altro. Ma, in ogni modo, tenta qualcosa”.
Può l’approccio “prova e sbaglia”, forse appropriato in economia e in politica, essere applicato anche alle decisioni mediche durante una pandemia? Non dovrebbero, invece, i medici accettare l’incertezza in modo razionale, mantenendo alta la guardia contro l’istintivo desiderio di trovare prove dove ci sono solo caso e coincidenze? Ivry Zagury‐Orly e Richard M. Schwartzstein si pongono queste domande in un recente editoriale del New England Journal of Medicine, opportunamente intitolato “A reminder to reason”: gli autori, entrambi dell’Harvard Medical School, invitano i medici a sorvegliare sui possibili errori cognitivi cui li espone la massiccia esposizione a informazioni in arrivo da fonti di varia affidabilità.
Il primo di essi è la cosiddetta euristica della disponibilità (in inglese availability bias), una scorciatoia mentale che fa condizionare il processo decisionale dalle informazioni più recenti e quindi più facilmente disponibili alla memoria; il secondo è il fissarsi sulla diagnosi di Covid-19 anche se i test non la confermano (“ci sono tanti falsi negativi!”) tralasciando, così, di esplorare la diagnosi differenziale; il terzo errore cognitivo è il confirmation bias, per cui si considerano più credibili le informazioni che avallano l’ipotesi preconcetta e si trascurano quelle che la contraddicono.
Terapie empiriche e danni collaterali
Sulla base di una loro efficacia in vitro o in altri contesti infettivi, sono state usate in tutto il mondo molte terapie empiriche per Covid-19 (clorochina, idrossiclorochina, azitromicina, lopinavir-ritonavir e inibitori dell’interleuchina 6), al di fuori di indicazioni e protocolli autorizzati, ma anche di sperimentazioni idonee a produrre prove scientifiche della loro efficacia in vivo. Tacendo dei potenziali danni collaterali di questi farmaci (tra cui aritmie cardiache e peggioramento delle infezioni), questo modo di prescrivere impedisce che si compiano reali passi avanti nella cura delle recidive dell’epidemia; vi sono allarmanti precedenti nell’epidemia da coronavirus SARS-CoV del 2003: gli studi mal condotti per mancanza di bracci di controllo non sono riusciti a distinguere gli effetti avversi da ribavirina e da cortisone dalle manifestazioni della malattia stessa.
Se, poi, sono in corso sperimentazioni formali, come lo studio clinico randomizzato e controllato e in cieco su remdesivir (un antivirale che potrebbe agire anche contro l’interleuchina 6), è bene resistere alla tentazione di comunicare risultati parziali o aneddotici, per salvaguardare l’utilità dei risultati definitivi. L’editoriale del NEJM esorta i medici a far prevalere la ragione sull’ansia di fare comunque qualcosa per i propri pazienti: il rischio è che l’agire clinico passi dall’imperativo ippocratico “primo, non nuocere” al pragmatismo impotente del “cosa abbiamo da perdere”.
L'iniziale allarme sugli ACE-inibitori
Un esempio dei guai che gli errori cognitivi citati dagli studiosi bostoniani possono portare con sé è l’allarme (per fortuna presto ridimensionato dalle principali società cardiologiche mondiali) che era scattato ai primi di marzo sulla potenziale pericolosità delle terapie antipertensive con ACE inibitori e sartani. Questi farmaci erano sospettati di facilitare l’infezione e di peggiorare il decorso di Covid-19, in base ad alcune osservazioni preliminari:
- il virus sfrutta l’ACE2 per entrare nelle cellule
- l’ACE2 è elevato nei soggetti in terapia con sartani e ACE inibitori
- i dati primi cinesi segnalano l’ipertensione tra i fattori di rischio nei pazienti con il maggior rischio di decesso
Come si sa, correlation is not causation: un editoriale del 18 marzo dell’European Heart Journal ha chiarito che probabilmente il fattore prognostico più sfavorevole è l’età avanzata e che ipertensione arteriosa, diabete mellito e cardiopatia ischemica sono il frequente corollario dell’invecchiamento. Il 17 aprile è stata pubblicata su Circulation Research un’analisi su oltre 3.611 pazienti affetti da Covid-19 nella provincia di Hubei, in Cina: 2.302 di loro non erano ipertesi e, dei 1.128 con pressione alta, solo 188 erano in terapia con ACE inibitori e sartani. Gli autori, per di più, hanno rilevato che la terapia con ACE inibitori e sartani riduceva:
- la frequenza di polmoniti bilaterali e dispnea
- la mortalità a 28 giorni per Covid (3,7% negli ipertesi trattati vs 9,8% nei non trattati)
- la mortalità per tutte le cause
- la percentuale di shock settico e di coagulopatia intravasale disseminata
Pur ammettendo i limiti di uno studio retrospettivo, è possibile trarne, quanto meno, una conclusione: gli ipertesi che assumono ACE inibitori e sartani possono continuare a farlo in tranquillità. Lo confermano anche due recentissimi studi: il primo, pubblicato sul NEJM a firma italiana, è uno studio caso controllo su 6.272 ammalati lombardi con grave sindrome respiratoria da SARS-CoV-2 e quasi 31.000 controlli. Nonostante il frequente politrattamento dei casi, l’indagine non ha trovato nessuna correlazione tra l’uso di questi antipertensivi e l’infezione o la sua evoluzione. Alla stessa conclusione è arrivato il secondo studio, pubblicato sul Lancet, che ha esaminato 1.139 ricoveri consecutivi per Covid-19 in 7 ospedali di Madrid e, come controlli, 11.390 ricoverati del 2018.
E se gli ACE-inibitori avessere un ruolo protettivo nei confronti di Covid-19?
Vale la pena di soffermarsi sulla possibilità (addirittura una probabilità, stando a un articolo del New England Journal of Medicine) inversa, ossia che i sartani abbiano un ruolo protettivo nei pazienti con Covid-19. Essa trae origine dal rapporto tra l’infezione virale e l’asse renina-angiotensina, che gli studi effettuati sull’epidemia da coronavirus SARS del 2002-2003, in parte simile all’attuale, hanno parzialmente chiarito. Il punto cruciale di questo rapporto è costituito dall’ACE2, l’Angiotensin-Converting Enzyme 2, identificato nel 2000 come punto di equilibrio della via che conduce all’angiotensina.
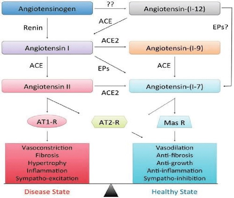
In sintesi, l’ACE2 controbilancia gli effetti negativi dell’angiotensina 2 (che si è formata per opera dell’enzima ACE a partire dall’angiotensina 1 quando si lega ai recettori AT1. Tale legame ha un ruolo nell’indurre ARDS (sindrome da distress respiratorio acuto), poiché:
- induce vasocostrizione e quindi ipoperfusione polmonare
- aumenta la permeabilità e quindi l’edema alveolare
- ha un’azione pro-infiammatoria sugli alveoli (alveolite)
- induce apoptosi delle cellule alveolari
- induce fibrosi connettivale (principale e più grave sequela dell’infezione)
L’ACE2 agisce da freno, convertendo l’angiotensina 2 in angiotensina 1-7, che, legandosi a recettori diversi, chiamati AT2 e Mas, determina effetti opposti: vasodilatazione, inibizione della fibrosi polmonare, azione antinfiammatoria e forse anche effetti antiaritmici e cardioprotettivi. Sia i farmaci ACE inibitori sia i sartani aumentano la disponibilità di livelli di ACE2, ma mentre gli ACE inibitori lo fanno bloccando l’azione dell’ACE (con conseguente riduzione dei livelli di angiotensina 2), i sartani bloccano direttamente il recettore AT1.
Come già dimostrato per il coronavirus precedente, anche il SARS-COV-2 si lega all’ACE2 presente nelle cellule alveolari: si potrebbe, quindi, ipotizzare che un aumento della disponibilità dell’ACE2 faciliti l’infezione e/o le sue complicanze polmonari. Si è visto, al contrario, che la maggiore gravità e letalità dell’infezione nei soggetti cardiopatici sono associate a bassi livelli di ACE2 e che l’infezione stessa da SARS-COV2 causa una riduzione dei livelli di ACE2.
In modelli murini è stato dimostrato che, a parità di stimolo lesivo alveolare, nei topi privi del gene che codifica per ACE2 il danno polmonare si estende più rapidamente e che i sartani attenuano il danno alveolare indotto dagli stimoli lesivi. Allo stesso modo, la diminuzione dell’ACE2 indotta dall’infezione da coronavirus può portare a un eccesso di angiotensina 2, che accelera il danno alveolare, agendo sui recettori AT1. Poiché i sartani bloccano l’azione dei recettori AT1, proprio quelli responsabili del danno alveolare, è possibile ipotizzare, anche nell’uomo, una loro azione protettiva dall’ARDS da Covid-19. Fatto salvo che i modelli animali non coprono tutte le varianti in gioco nella clinica umana, il possibile effetto benefico di questa classe di farmaci vale la pena di essere indagato.
Bibliografia
Mancia G et al. Renin–angiotensin–aldosterone system blockers and the risk of Covid-19. New Engl J Med May 1, 2020 DOI: 10.1056/NEJMoa2006923
Zhang P et al. Association of Inpatient Use of Angiotensin Converting Enzyme Inhibitors and Angiotensin II Receptor Blockers with Mortality Among Patients With Hypertension Hospitalized With COVID-19 [published online ahead of print, 2020 Apr 17]. Circ Res. 2020;10.1161/CIRCRESAHA.120.317134
Zhang H et al. Recombinant human ACE2: acing out angiotensin II in ARDStherapy. Crit Care. 2017 Dec 13;21(1):305
Zheng YY et al. COVID-19 and the cardiovascular system. NatRev Cardiol. 2020 Mar 5
Imai Y et al. The discovery of angiotensin-converting enzyme 2and its role in acute lung injury in mice. Exp Physiol. 2008 May;93(5):543-8
Hoffmann M et al. SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a ClinicallyProven Protease Inhibitor. Cell. 2020 Mar 4
Chamsi-Pasha MA et al. Angiotensin-converting enzyme 2 as atherapeutic target for heart failure. Curr Heart Fail Rep. 2014; 11: 58-63
Kuba K, Imai Y, Penninger JM. Angiotensin-converting enzyme 2 in lung diseases. Curr Opin Pharmacol. 2006; 6: 271-76
Imai Y et al. Angiotensin-converting enzyme 2 protects from severe acute lungfailure. Nature 2005; 436: 112-16
Kuster GM et al. SARS-CoV2: should inhibitors of the renin-angiotensin system be withdrawn in patients with COVID-19? [published online ahead of print, 2020 Mar 20]. Eur Heart J. 2020;ehaa235. doi:10.1093/eurheartj/ehaa235
Sun P et al. Clinical characteristics of 50466hospitalized patients with 2019-nCoV infection. J Med Virol. 2020 Feb 28
Schouten LR et al. for MARS consortium. Age-dependent differences in pulmonaryhost responses in ARDS: a prospective observational cohort study. Ann IntensiveCare. 2019 May 14;9(1):55
Ferrario CM et al. Effect of angiotensin-converting enzyme inhibition andangiotensin II receptor blockers on cardiac angiotensin-converting enzyme 2. Circulation 2005; 111: 2605-10
Liu L et al. Losartan, an antagonist of AT1receptor for angiotensin II, attenuates lipopolysaccharide-induced acute lunginjury in rat. Arch Biochem Biophys. 2009; 481: 131-36
Gurwitz D. Angiotensin receptor blockers as tentative SARS-CoV-2 therapeutics. Drug Dev Res. 2020 Mar 4. doi: 10.1002/ddr.21656
Vaduganathan M et al. Renin-Angiotensin-Aldosterone System Inhibitors in Patients with Covid-19. N Engl J Med. 2020 Apr 23;382(17):1653-1659. doi: 10.1056/NEJMsr2005760
Watkins J. Preventing a covid-19 pandemic. BMJ. 2020 Feb 28;368:m810
Wang D et al. Renin-angiotensin-system, a potential pharmacological candidate, in acute respiratory distress syndrome during mechanical ventilation. Pulm Pharmacol Ther 2019; 58: 101833
de Abajo F et al. Use of renin–angiotensin-aldosterone system inhibitors and risk of COVID-19 requiring admission to hospital: a case-population study. www.thelancet.com14, 2020 https://doi.org/10.1016/ S0140-6736(20)31030-8

