
Crediti: PublicDomainPictures/Pixabay. Licenza: Pixabay License
Il termine “sicurezza”, utilizzato per i farmaci, è spesso ambiguo. Sicurezza avrebbe il significato di “non generare problemi” che in gergo significano effetti collaterali, per usare un eufemismo in luogo di effetti tossici. Tuttavia, è noto che non esistono farmaci innocui, al contrario tutti i farmaci attivi hanno una contropartita di effetti indesiderabili. Il termine sicurezza va perciò confrontato con il termine “beneficio”. Infatti, come per qualsiasi altro intervento, si possono accettare le forme più o meno importanti di tossicità solo in cambio di benefici per la propria salute.
Più che di sicurezza nel prosieguo parleremo del suo opposto, ovvero del rischio di tossicità, un termine negativo che non è molto amato dal mercato dei farmaci. Infatti, quando si studia un nuovo farmaco nelle varie fasi precliniche, i modelli animali sono tutti orientati a valutare il beneficio e solo alla fine dello studio si cerca di valutare la tossicità cronica, spesso in esperimenti di durata relativamente breve, rinviando a tempi successivi la ricerca di tossicità più specifiche, quali ad esempio la mutagenesi, cancerogenesi e le anomalie della riproduzione. Negli studi clinici l’obiettivo è fondamentalmente quello di stabilire i benefici. Infatti, la numerosità del campione viene calcolata per ottenere un dato statisticamente significativo del beneficio atteso e non per valutare il livello di tossicità.
Il termine stesso di beneficio viene dilatato per includere parametri che rappresentano un beneficio “surrogato”. Infatti, un farmaco spesso si valuta per la sua capacità di ridurre la pressione, il colesterolo, la glicemia e altri parametri biochimici, assumendo - ma non sempre dimostrando - che questi siano indicatori di vantaggi terapeutici per il paziente. L’impiego di un farmaco non viene sempre valutato per i parametri importanti per la salute quali la morbilità, la mortalità o la qualità di vita. Mentre l’efficacia si ricerca, la tossicità si… attende! Infatti, non esiste un programma specifico di farmacovigilanza attiva; gli effetti tossici vengono raccolti dalle informazioni spontanee di medici, farmacisti, infermieri e pazienti e quindi sono certamente dati sottostimati, soprattutto quando gli effetti tossici avvengono a distanza di tempo rispetto alla somministrazione dei farmaci. La mancanza di sorveglianza sugli effetti tossici rende necessario, anche dopo molti anni dalla commercializzazione il ritiro dei farmaci. È sintomatico che spesso i farmaci vengano ritirati dal commercio dalle industrie anziché dalle autorità regolatorie1.
Tossicità
Come già accennato il mercato della medicina tende a privilegiare i benefici. Ad esempio, solo poche riviste si occupano di tossicologia farmaceutica: un’indagine condotta sulle principali riviste mediche mostra che solo l’1,5% degli articoli si occupa delle reazioni avverse. Lo stesso studio della tossicologia è visto come un’attività di ricerca minore. Grande enfasi invece viene data a studi che rilevino qualsiasi beneficio, per quanto piccolo.
La tossicità da farmaci non è affatto trascurabile. Si calcola infatti che negli USA il 70% delle ammissioni ospedaliere siano determinate da pazienti con età eguale o superiore a 65 anni che assumono cinque o più farmaci al giorno; mentre in Europa si ritiene che ogni anno vi siano 8,6 milioni di ammissioni ospedaliere dovute alle reazioni avverse da farmaci (Report NHS Scotland). Per quanto riguarda l’Italia gli studi sono poco numerosi e molto incompleti, perché basati essenzialmente su rapporti spontanei. Ad esempio, nel rapporto AIFA2 su oltre 300 pagine riguardanti spesa e consumo di farmaci non esiste un solo capitolo sulla tossicità dei farmaci. Si menzionano solo alcuni dati indiretti nel rapporto Osmed 2016 che dedica sette pagine agli eventi avversi.
La tendenza attuale a registrare con maggiore rapidità (fast track) i farmaci promettenti tende a ritardare la conoscenza degli effetti tossici. Ad esempio dati FDA riportano che per i farmaci approvati precocemente si devono in seguito riportare nella scheda tecnica il 48% in più di effetti collaterali rispetto ai farmaci approvati con i tempi normali. È stato anche riportato che l’utilizzo inappropriato di farmaci aumenta di due volte i ricoveri ospedalieri, con particolare riferimento nei soggetti anziani. I risultati dello Studio REPOSI3 condotto in Italia sono coerenti con questi dati, dimostrando che soggetti anziani che assumono più di cinque farmaci hanno una mortalità tre volte superiore, spesso dovuta a gravi interazioni tra farmaci. Le reazioni avverse sono di fatto più numerose in rapporto al numero di farmaci assunti4.
Poco nota è l’incidenza della tossicità in rapporto con il genere. Un rapporto della FDA indica che gli effetti avversi nelle donne assommavano a 2 milioni quando nel maschio erano limitati a 1,3 milioni5. Come accade anche per i benefici, a maggiore ragione per gli effetti tossici molti studi clinici controllati non includono un numero adeguato di donne6 e perciò spesso non riportano le percentuali di tossicità in rapporto al genere7.
Le dosi dei farmaci rispetto al peso corporeo sono in generale più alte nella femmina rispetto al maschio. Questo assieme alle differenze nel metabolismo dei citocromi P450 epatici può essere causa di molti casi di maggior tossicità nella donna8,9. Un caso del genere è rappresentato dagli antipsicotici per quanto riguarda reazioni avverse di tipo metabolico10.
È interessante dare alcuni esempi di farmaci per cui sono poco propagandati gli effetti tossici. L’enfasi indubbiamente giustificata data ai nuovi medicamenti antitumorali che agiscono su base immunitaria non è stata accompagnata da un’adeguata informazione sulle reazioni autoimmunitarie che si evidenziano anche a distanza di tempo11. In seguito all’impiego di questi farmaci, il WHO ha riportato 101 casi di miocardite fulminante12,13.
Sempre per dare alcuni esempi, senza essere esaustivi, si possono anche ricordare farmaci che hanno effetti avversi molto gravi rispetto alla loro reale utilità. Fra gli uricosurici, il febuxostat, pur non essendo più attivo dei farmaci già disponibili come l’allopurinolo, induce un aumento del 22% della mortalità da tutte le cause e una mortalità cardiovascolare del 32% più alta14. Gli antagonisti dell’endotelina, utilizzati per la terapia dell’ipertensione polmonare, inducono un aumento del 60% di malattie cardiovascolari e dell’80% dell’anemia15 rispetto ai controlli.
Gli estrogeni associati ad alcuni progestinici come il levonorgestrel aumentano del 26% la probabilità di avere un embolismo polmonare16. I farmaci antidepressivi, urologici e antiparkinson che esercitano effetti anticolinergici aumentano la probabilità di demenza senile anche se somministrati 20 anni prima17.
Molto spesso anche i benefici possono essere vanificati dall’incidenza di reazioni avverse. Ad esempio, si è osservato che preparati di cannabis sono in grado di diminuire la spasticità nell’ammalato di sclerosi multipla, ma nel suo complesso la qualità di vita non è modificata, probabilmente a causa degli effetti avversi della cannabis sul sistema nervoso centrale18.
Efficacia
È impossibile valutare il significato delle reazioni avverse senza considerare quali siano veramente i benefici. Infatti, mentre è possibile giustificare anche rischi gravi a fronte di un effetto fortemente positivo, è difficile accettare reazioni avverse anche modeste di farmaci che non abbiano vantaggi rispetto a farmaci già esistenti.
La stessa legislazione europea non favorisce certo la possibilità di valutare i reali benefici, perché per l’approvazione di un nuovo farmaco vengono richieste solo tre caratteristiche: “qualità, efficacia e sicurezza” il che vuol dire che ogni farmaco viene giudicato per se stesso, come se non esistessero nella maggior parte dei casi già altri farmaci con le stesse indicazioni cliniche. Diversa sarebbe la situazione se la legge prescrivesse: “qualità, efficacia, sicurezza e valore terapeutico aggiunto”. In tal caso sarebbe necessario fare studi comparativi e verrebbero perciò approvati solo farmaci con caratteristiche di migliore efficacia o minore tossicità rispetto a quelli esistenti. Se ciò accadesse, in molti casi sarebbe necessario rimuovere dal mercato i vecchi farmaci superati dai nuovi.
Il risultato dell’attuale legislazione è la presenza sul mercato di molti farmaci che in realtà rispondono più agli interessi delle industrie farmaceutiche rispetto a quelli degli ammalati. Un gruppo di esperti della rivista Prescrire ha valutato l’efficacia clinica dei farmaci approvati in Europa negli ultimi dieci anni (2008-2017). Il risultato non è entusiasmante perché su 943 farmaci e indicazioni terapeutiche esaminati, solo 58 rappresentano, per ragioni diverse, un reale progresso terapeutico, mentre 662 erano classificati come inutili o non accettabili. Inoltre, 223 prodotti rimanevano in attesa di giudizio perché il loro rapporto beneficio-rischio era ancora difficilmente valutabile (tabella 1).
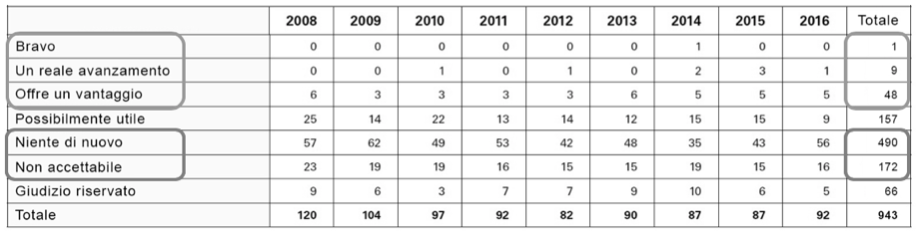
Tabella 1 Classificazione dei nuovi farmaci e delle nuove indicazioni approvate dall’EMEA da parte della rivista Prescrire
Un problema particolare è rappresentato dai farmaci antitumorali, spesso approvati certamente con l’idea che siano utili. Ma spesso la loro approvazione, in assenza di adeguate evidenze scientifiche, crea solo confusione. Ad esempio, l’EMA, l’organismo europeo che approva i nuovi farmaci, ha autorizzato nel periodo di quattro anni (2009-2013) ben 68 nuovi farmaci antitumorali. Tuttavia, per il 57% (39/68) di questi non esistevano evidenze di aumento della sopravvivenza degli ammalati trattati. Secondo altri autori19 solo 24 farmaci su 68 mostravano un significativo aumento della sopravvivenza con una mediana di 2,7 mesi. Dopo circa sei anni solo 6 farmaci su 39 avevano ottenuto risultati positivi20. L’approvazione precoce crea problemi, perché poi risulta difficile eseguire studi clinici controllati rispetto ad altre terapie e spesso i nuovi farmaci vengono utilizzati impropriamente come standard per studi di confronto.
Approvare tanti farmaci in tempi brevi crea grande confusione fra gli oncologi, perché per molti prodotti la disponibilità del farmaco è accompagnata solo da approssimative conoscenze circa le dosi, la durata del trattamento, la combinazione con altri farmaci e soprattutto un’adeguata conoscenza del rapporto benefici-rischi.
Per discutere dei benefici, come della tossicità, si deve tener conto delle modalità con cui vengono acquisite le conoscenze. Negli studi clinici controllati si fanno confronti fra il nuovo trattamento e il placebo o un farmaco di riferimento. Alla fine di un certo periodo di trattamento si valutano i benefici e le tossicità attraverso l’impiego della statistica. I risultati indicano perciò il beneficio nella popolazione trattata, ma non possono evidenziare chi ha beneficiato del trattamento o chi ne è stato penalizzato. Quando ci si accinge a fare una prescrizione, il paziente, dovrebbe sapere qual è la probabilità di avere un beneficio, perché raramente un farmaco porta benefici al 100% dei trattati. Una modalità per esprimere questa probabilità è il numero di pazienti che devono essere trattati, perché uno abbia un beneficio terapeuticamente significativo (NNT).
Impiegando l’evolocumab, un nuovo farmaco che agisce come un potente ipocolesterolemizzante, per ogni mille pazienti trattati si ottengono, rispetto ai controlli, 15 casi in meno di morte cardiaca, infarto miocardico o ictus cerebrale. Ciò vuol dire che su 1.000 pazienti 926 vengono trattati inutilmente perché non avrebbero avuto alcun evento cardiovascolare, 59 hanno comunque avuto il danno pur essendo trattati e 15 appunto sono stati beneficati. In definitiva, bisogna perciò trattare 66 pazienti (NNT) affinché uno abbia un vantaggio. È chiaro che questa probabilità ha un significato diverso per chi abbia un rischio cardiovascolare alto o basso, per chi sia giovane o anziano, maschio o femmina21.
Lo stesso approccio si dovrebbe avere non solo per valutare il beneficio, ma anche per sapere quanti pazienti è sufficiente trattare perché si manifesti una determinata forma di tossicità (NNH). Ad esempio, l’impiego dell’aspirina in prevenzione primaria ha un NNT = 522, cioè bisogna trattare molti pazienti per prevenire un infarto; ma il modesto vantaggio si rivela in realtà uno svantaggio se si considera il NNH = 111 per gravi effetti avversi22.
La tabella 2 permette di avere un’idea degli NNT per l’alendronato, un farmaco utilizzato per ridurre le fratture dopo la menopausa. Tali dati possono ovviamente cambiare in rapporto con l’obiettivo terapeutico, le dosi, i tempi di somministrazione, il genere e l’età del paziente. È chiaro che la personalizzazione dei trattamenti richiederebbe di sapere chi può avere vantaggio dalla somministrazione del farmaco per evitare che molti altri ricevano trattamenti inutili o addirittura dannosi.
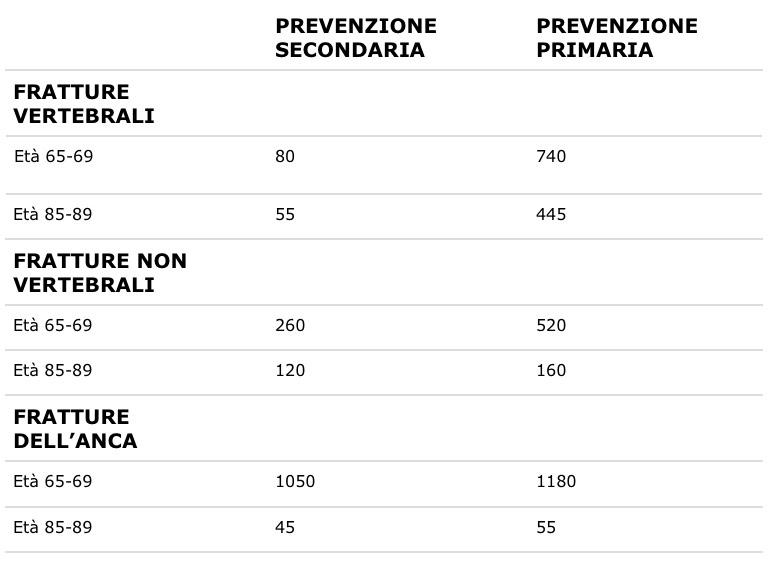
Tabella 2 NNT per l’alendronato in rapporto con l’età e il tipo di frattura
Quanti medici nel prescrivere un farmaco hanno presente il NNT per il risultato che si vuole ottenere e quanti pazienti ricevono questa informazione per fornire il proprio consenso consapevole al trattamento?
Infine, occorre ricordare che molti dei dati riportati sono ottenuti in condizioni sperimentali. Diversa è la situazione nella realtà clinica, quando i pazienti sono sottoposti contemporaneamente al trattamento con molti farmaci. Il già citato Studio REPOSI, condotto in Italia e Spagna, raccoglie le caratteristiche dei pazienti ricoverati nei dipartimenti di medicina interna. La tabella 3 dà un’indicazione del numero di pazienti trattati con più di cinque farmaci nel corso degli anni, all’ammissione e alla dimissione dall’Ospedale. È chiaro che con tanti farmaci il numero di interazioni è incalcolabile e ancor meno è quantificabile il rapporto benefici-tossicità.
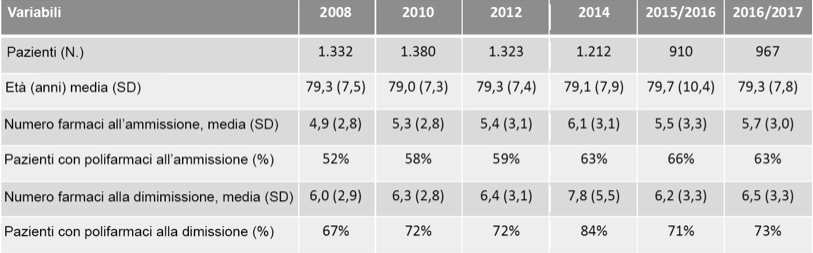
Tabella 3 Studio Reposi. (dati raccolti a settembre 2017). Caratteristiche della coorte. Polifarmaci = 5 o più farmaci/giorno
La spesa farmaceutica
In Italia sono in commercio ben 16.247 medicinali. Di questi 10.341 sono rimborsati dal Servizio Sanitario Nazionale (SSN) da parte della medicina territoriale o delle strutture ospedaliere pubbliche e convenzionate. Questi farmaci hanno comportato una spesa totale di 29,811 miliardi di euro di cui 22,555 miliardi rimborsati dal SSN, comprendenti 10,495 miliardi di euro relativi alla spesa territoriale dei medici di medicina generale. I dettagli della spesa pubblica e privata sono riportati nella Tabella n. 4 che indica anche la differenza di spesa nel 2017 rispetto al 2016. La spesa farmaceutica è in continuo aumento e nel triennio 2013-2016 ha utilizzato ben 2,046 miliardi di euro rispetto ai 2,866 messi a disposizione dal Governo per incrementare il Fondo Sanitario Nazionale, che per il 2017 assommava a circa 113 miliardi di euro. In realtà, la spesa farmaceutica a carico del SSN raggiunge circa il 20%, dato questo forse leggermente sottostimato. È lecito chiedersi se questa cifra sia veramente proporzionale ai benefici che si ottengono rispetto ai rischi, come si è visto nei precedenti capitoli.
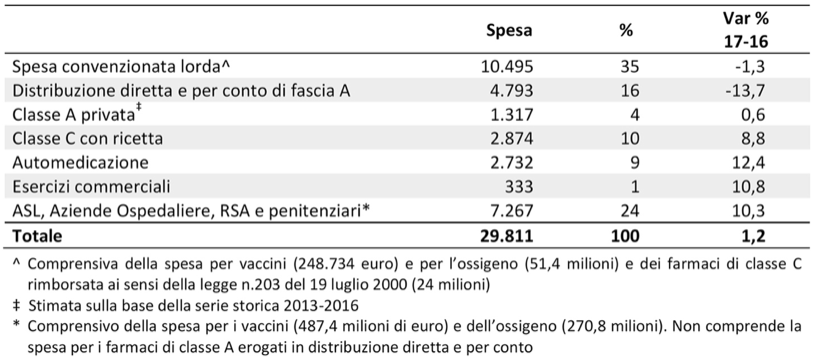
Tabella 4 Composizione della spesa farmaceutica in milioni di euro: confronto 2017-2016
La spesa farmaceutica è governata in Italia da un’agenzia, AIFA (Agenzia Italiana del Farmaco), che ha una duplice funzione: mettere a disposizione del mercato generale (fascia C) tutti i farmaci approvati dall’EMA (European Medicines Agency) a carico del pubblico senza interferire sui prezzi proposti dai produttori e selezionare fra questi farmaci quelli rimborsabili dal SSN, contrattandone i prezzi con le industrie farmaceutiche interessate.
Come si è già osservato, la maggioranza dei farmaci, anche quelli disponibili per il SSN, sono in generale delle fotocopie di quelli già esistenti, anche se possono avere strutture chimiche differenti, perché non vengono realizzati adeguati studi comparativi. Gli stessi principi attivi sono spesso presenti in un numero eccessivo di prodotti e di confezioni, il che genera una forte offerta, non sempre necessaria. Non solo ma, come si può osservare dalla tabella 4, principi attivi uguali hanno prezzi differenti, come pure principi con le stesse indicazioni hanno prezzi considerevolmente differenti, senza che vi siano dimostrazioni di maggior efficacia o di minore tossicità.
Proposte
È chiaro che il mondo dei farmaci richiede cambiamenti significativi per evitare che il mercato prevalga sugli interessi degli ammalati, in particolare per quanto riguarda il Servizio Sanitario Nazionale. Poiché in Italia è l’AIFA incaricata, fra l’altro, di stabilire quali farmaci debbano essere forniti gratuitamente agli italiani, è a questo organismo che vanno indirizzate tutte le proposte.
Anzitutto, da un punto di vista della policy, l’AIFA dovrebbe sposare l’impostazione del “valore terapeutico aggiunto” e quindi considerare i prodotti approvati dall’EMA come un catalogo da cui attingere i farmaci che sulla base dell’evidenza scientifica rappresentano un reale vantaggio. Ma se un farmaco implica per una certa indicazione un vantaggio rispetto a quelli esistenti, è logico che altri farmaci escano dal Prontuario. Ciò implica da un lato una continua revisione del Prontuario Terapeutico e dall’altro un’assunzione di responsabilità che va chiaramente identificata. Attualmente abbiamo in AIFA un Consiglio di Amministrazione, un Direttore che ha la rappresentanza legale, una Commissione Tecnico-Scientifica (CTS) fatta da esperti che stabiliscono se il farmaco è rimborsabile e un Comitato Prezzi e Rimborsi (CPR) che contratta i prezzi con i produttori. Forse sarebbe utile snellire questi Comitati, consultare molto di più gli esperti nei campi specifici di utilizzazione del farmaco in questione e ritornare a una CUF (Comitato Unico del Farmaco) che riunisca CTS e CPR.
Per mantenere l’indipendenza di giudizio, AIFA non dovrebbe avere conflitti di funzione. Ad esempio, non dovrebbe dare “consigli scientifici” sui clinical trial che poi devono essere giudicati dalla stessa organizzazione. Per la stessa ragione, AIFA non dovrebbe essere l’organismo competente per validare gli studi clinici controllati e non dovrebbe essere sede del Comitato Nazionale di Coordinamento dei Comitati Etici regionali.
Una funzione fondamentale per l’immediato dovrebbe essere la revisione sistematica del Prontuario Terapeutico Nazionale, cosa che non avviene dal 1993, cioè da 25 anni. Altre regole importanti riguardano alcune decisioni da prendere in modo generalizzato. Ad esempio, farmaci con lo stesso principio attivo devono avere lo stesso prezzo, come pure farmaci con la stessa indicazione. Nella situazione di farmaci ad alto costo dovrebbe essere richiesto di giustificare il prezzo. All’aumentare dei volumi di prescrizione dovrebbe corrispondere una diminuzione del prezzo per tutti i farmaci che appartengono allo stesso gruppo.
In questo modo non ci dovrebbero essere incentivi o situazioni speciali per farmaci innovativi, perché tutti i farmaci ammessi alla rimborsabilità devono essere per le ragioni suddette innovativi. Possono essere ammessi farmaci-copia (me-too) nel caso abbiano un prezzo considerevolmente inferiore a quelli esistenti, perché in quel caso verrebbero abbassati anche i prezzi dei farmaci appartenenti allo stesso gruppo.
Le confezioni devono essere adeguate ai tempi di terapia per evitare inutili sprechi. Va considerata anche la possibilità di realizzare aste nazionali per i prodotti di uso più comune. Sembra strano sottolineare questi aspetti, considerando che rappresentano le modalità con cui agiscono tutte le aziende commerciali o industriali indipendentemente dalle loro attività.
Un compito importante dell’AIFA, quasi completamente assente in questo momento, è l’informazione. Non è possibile che tutta l’informazione sui farmaci sia monopolio dell’industria farmaceutica. È necessario un costante, giornaliero impegno di informazione per tutti i medici che appartengono al SSN, perché conoscano attraverso gli NNT e gli NNH la reale efficacia e la tossicità dei farmaci, non trascurando informazioni sui prezzi e soprattutto sulle interazioni fra farmaci. Gli informatori farmaceutici dell’industria non dovrebbero avere accesso diretto ai medici, ma dovrebbero avere la possibilità di svolgere seminari collettivi sui loro prodotti, magari con contraddittorio. È necessario che tutti i medici appartenenti al SSN abbiano idee chiare sui farmaci e soprattutto sull’equivalenza dei prodotti generici e biosimilari rispetto ai prodotti originali. La libertà di prescrizione ha un significato solo quando il medico può fare scelte fra prodotti diversi e non fra prodotti dichiarati equivalenti dall’autorità regolatoria.
Infine, last but not least, esiste l’assoluta necessità di intensificare la ricerca indipendente (vedi la tabella 5 per le sue caratteristiche rispetto alla ricerca industriale) il cui finanziamento deve contare su almeno l’1% del budget del SSN, con tendenza al 3%. Questa ricerca è fondamentale per caratterizzare i farmaci in base a dosi ottimali e a tempi di trattamento adeguati. Sono fondamentali studi comparativi per dare utili informazioni all’AIFA, nonché studi che permettano di stabilire, soprattutto per la terapia antitumorale, quali siano le combinazioni di farmaci più efficaci e meno tossiche. Va ristabilita l’asimmetria benefici-rischi, promuovendo studi di farmacovigilanza “attiva”. I farmaci sono fondamentali quando vengono utilizzati in modo appropriato. Occorre evitare che i farmaci per ragioni di mercato siano considerati beni di consumo anziché strumenti di salute.
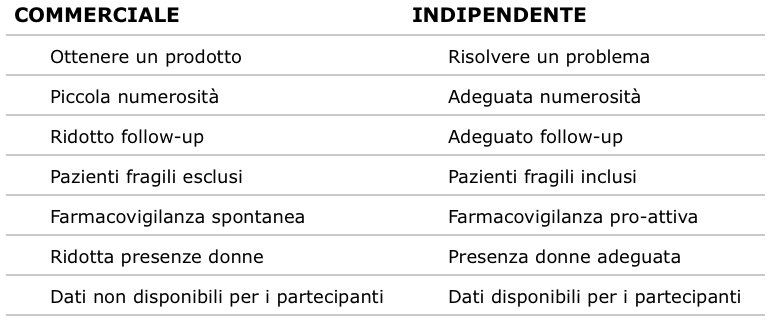
Tabella 5 Differenze nella ricerca clinica commerciale e indipendente

